Il sito web V-safe dei Centri per il controllo e la prevenzione delle malattie (CDC) ha smesso silenziosamente di raccogliere segnalazioni di eventi avversi senza motivo o spiegazione. Il sito web V-safe semplicemente stati"Grazie per la vostra partecipazione. La raccolta dei dati per i vaccini COVID-19 si è conclusa il 30 giugno 2023.” Se ci vai oggi, V-safe indirizza gli utenti al sito web VAERS della FDA per la segnalazione degli eventi avversi i funzionari deridevano continuamente il VAERS definendolo “passivo” e “non verificato”.

VAERS e V-safe sono database di raccolta di dati di sicurezza reciprocamente esclusivi gestiti rispettivamente dalla FDA e dal CDC. VAERS è un modo più antico di raccogliere dati sulla sicurezza in cui è possibile compilare un modulo online, manualmente o chiamando un numero verde, mentre V-safe è una "app" del dispositivo che richiede la registrazione online. Sia VAERS che V-safe raccolgono informazioni personali, numeri di lotto, date e informazioni associate, ma V-safe era un sistema di raccolta attivo rivolto a un gruppo demografico più giovane che utilizzava le app.
Ecco l'ultimo rapporto prima della cancellazione.
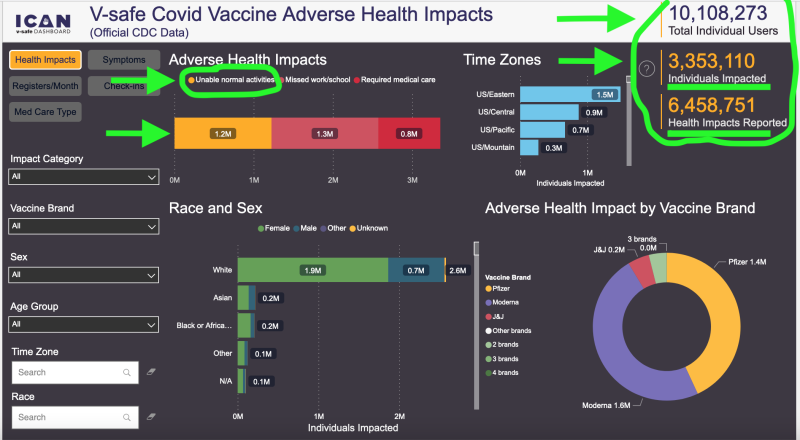
Ciò significa che il CDC ritiene che le iniezioni di mRNA Covid-19 siano così sicure che non è più necessario monitorare le segnalazioni di eventi avversi? Qual è l'argomento contro un monitoraggio continuo, soprattutto dal momento che il sito web V-safe era già attivo e pagato?
Mentre il V-safe del CDC è stato spento di nascosto e all'improvviso, rifiutandosi di accettare nuovi rapporti sulla sicurezza, fino ad oggi il CDC continua a esortare tutti coloro dai 6 mesi in su a restare aggiornati con vaccini e richiami anti-COVID-19.
In qualità di esperto di sicurezza dei farmaci, personalmente non posso citare un altro esempio di agenzia o produttore che ha interrotto la raccolta di dati sulla sicurezza. Sembra ancora peggio perché la tecnologia dell'mRNA è relativamente nuova e le manifestazioni a lungo termine sono sconosciute. In cima a questa, sia i produttori che la FDA si rifiutano di condividere , il elenco di ingredienti, come le nanoparticelle lipidiche, che potrebbero influenzare gli individui in modo diverso e richiedere molto tempo per manifestarsi clinicamente.
La raccolta dei dati sulla sicurezza non dovrebbe mai fermarsi
Ora, confrontalo con il fatto che la National Highway Traffic and Safety Administration (NHTSA) accetterà comunque un rapporto sulla sicurezza un Ford Bronco II di 30 anni. In effetti, questo è un esempio stranamente specifico, ma solo perché ho guidato esattamente questo veicolo come una famiglia tramandata da studente, attraverso la mia residenza, borsa di studio, per il mio mandato come Professore di Yale nelle cattive strade di New Haven e anche durante i miei anni alla FDA come ufficiale medico/analista medico senior.
Come le iniezioni di mRNA, i Bronco II sono ancora disponibili sul mercato e le persone li usano ancora oggi. Il mio Bronco è diventato un argomento di conversazione intermittente con amici e colleghi della FDA. Un giorno, una guardia di sicurezza di pattuglia presso la FDA mi informò che era l'auto più vecchia del campus.
All'epoca non sapevo molto di automobili (o della tecnologia mRNA), ma quando un collega membro della FDA mi informò che il mio Bronco II aveva notevoli problemi di sicurezza e che l'NHTSA teneva ancora gli occhi puntati su questo veicolo (gli incidenti di cappottamento erano più comuni e più mortali) ho affrontato il problema: mi sono sbarazzato dell'affidabile reliquia, anche se veramente piaciuto esso.
L'NHTSA sta ancora accettando rapporti sulla sicurezza su cose come il mio Ford Bronco II di 30 anni, ma il CDC non accetta nuovi rapporti sulla sicurezza su nuovi vaccini a mRNA vecchi di 2 anni.

Il CDC non accetta più rapporti sulla sicurezza nonostante il rapido aumento dei risultati sulla sicurezza:
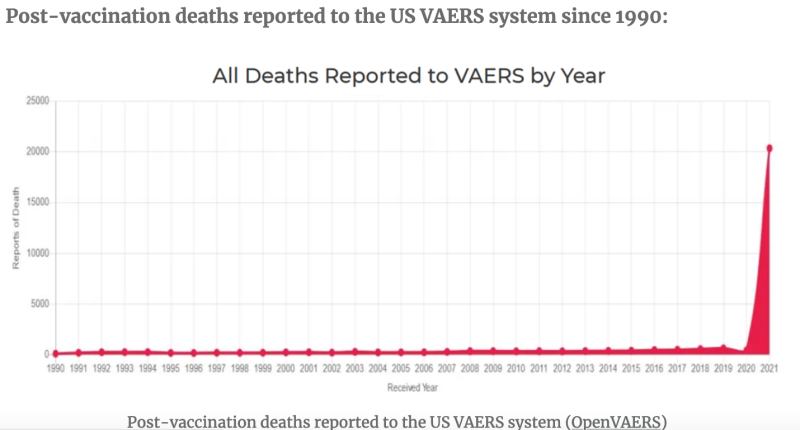
A differenza del mio vecchio Bronco, le iniezioni di mRNA sono sul mercato solo da circa seconda anni e, secondo il database VAERS (Vaccine Adverse Event Reporting System) della FDA, i “vaccini” mRNA sono stati nominati primario sospettato di oltre 1.5 milioni di segnalazioni di eventi avversi, di cui ci sono >20,000 attacchi di cuore ed >27,000 casi di miocardite e pericardite solo negli Stati Uniti. I numeri mondiali sarebbero maggiori. Secondo molti riferimenti, incluso uno studio di Harvard finanziato dalla FDA, I rapporti VAERS rappresentano meno dell’1% degli eventi avversi da vaccino che effettivamente si verificano.
È interessante notare che la Collegamento NHTSA sopra sul mio Ford Bronco II mostra solo: prima richiamo di parti, prima indagini e 23 reclami, e presenta ancora un pulsante nell'angolo in alto a destra per inviare nuovi reclami.
Wikipedia definisce un crisi umanitaria o disastro umanitario come: “evento singolo o una serie di eventi che mettono a rischio la salute, la sicurezza o il benessere di una comunità o di un ampio gruppo di persone”. Sulla base del VAERS e dei precedenti risultati di V-safe, gli eventi avversi derivanti dalle iniezioni di mRNA solo negli Stati Uniti potrebbero essere considerati una crisi umanitaria.
Nonostante questi risultati clinici allarmanti, il CDC ha concluso che la raccolta di nuovi rapporti sulla sicurezza in qualche modo non è più nell’interesse della salute pubblica americana. I dati esistenti dal sito V-safe sono stati mostrati in giro 6.5 milioni di eventi avversi/impatti sulla salute su 10.1 milioni di utenti, di cui circa 2 milioni non sono in grado di svolgere le normali attività della vita quotidiana o necessitano di cure mediche, secondo i risultati di una terza parte. In altre parole, nonostante le iniezioni di mRNA siano ancora ampiamente disponibili e il CDC ne promuova l'uso continuato, il caso è “chiuso” per quanto riguarda la raccolta di nuovi rapporti sulla sicurezza, sotto l'odierna amministrazione federale della sanità pubblica.
Il CDC si esprimerà sui dati esistenti o giustificherà la sua interruzione nella raccolta di nuovi dati sulla sicurezza? Per quanto ne so, fermare la raccolta di informazioni sulla salute pubblica non ha una giustificazione clinica o una precedenza scientifica, soprattutto quando si tratta di un prodotto commercializzato attivamente.
In George Orwell's 1984, Il Partito ha detto ai personaggi di "rifiutare l'evidenza dei tuoi occhi e delle tue orecchie". Ora, il CDC non consente nemmeno che tali prove vengano raccolte per la visualizzazione (e l'eventuale rifiuto). È un'idea terribile per in qualsiasi prodotto, per non parlare delle nuove tecnologie di mRNA.
Pubblicato sotto a Licenza internazionale Creative Commons Attribution 4.0
Per le ristampe, reimpostare il collegamento canonico all'originale Istituto di arenaria Articolo e Autore.









